Definer hydrogenbinding
Hydrogenbindinger er severdigheter som følge av dipol avgifter mellom electro hydrogen og et sterkt elektronegativt atom (oksygen, nitrogen eller fluor) kovalent bundet til den. Dette kan omtrent sammenlignes med nord og sør poler av en magnet. Nord tiltrekker sør. Positive tiltrekker negative. I den ene enden av et dipolart molekyl, er det en liten positiv ladning, og i den andre enden, en liten negativ ladning. Samlet, men det er ingen netto kostnad. Den enkleste og mest viktig eksempel på hydrogenbinding er at det mellom to eller flere vann (H₂O) molekyler.
polaritet
Vann er bipolart fordi det ikke synes helt nøytral til "omverdenen". Siden oksygen er electro, pleier det å trekke elektroner bort fra sine to hydrogenatomer, vedta en netto minus kostnad. På grunn av dette, hydrogenatomene som hver bærer en liten positiv ladning.
Styrke
Selv om de ikke er full kostnader, men bare delvis de, andre atomer, også med små kostnader, trekkes til dem. De resulterende obligasjoner kalles hydrogenbindinger. Disse obligasjonene er ikke så sterk som kovalente eller ioniske bindinger, men de er uhyre viktig.
En utmerket Shockwave animasjon av Northland Fellesskapet & Technical College (demonstrere dannelsen i vann av hydrogenbindinger) er sitert nedenfor. Det viser hvordan vannmolekyler justere seg selv for å danne en nettstruktur.
Vannmolekylene beholde egen identitet, selv om de grupperes eller "knytte". Hvert molekyl av vann kan danne opp til fire hydrogenbindinger.
Betydning
Den første og mest åpenbare betydning er funnet i vann, selv. Hydrogenbinding fører vann til å koke ved en temperatur vesentlig høyere enn den ellers ville. Dette hindrer rask fordampning, en tørking av havene, og tap av alt liv.
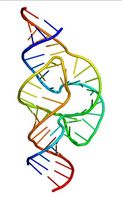
Hydrogenbinding tillater dannelse av såkalte "tertiær struktur" (som eksempel, se figur 1). Svært store biomolekyler har konkrete romlige orienteringer i stor grad på grunn av hydrogenbinding.
proteiner
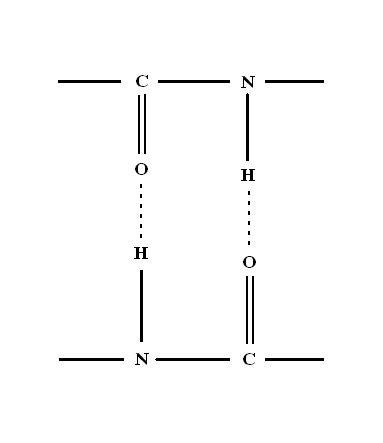
Proteiner er et utmerket eksempel på hvorfor dette er. Signaturen amidbindingen av proteiner kan justere to proteinmolekyler (figur 2). Slike justeringer ikke alltid krever ulike molekyler. Mye signifikant hydrogenbinding kommer fra et enkelt molekyl.
Når multiplisert en rekke ganger i løpet av ordinær måte i store molekyler, disse justeringer produsere helikser og ark avgjørende for livet. "Double helix" av DNA illustrerer godt poenget.
kosmetisk
Hydrogenbinding er vesentlige for livet, ja. Det kan også legge skjønnhet til livet. Evnen til å krølle håret foreligger, delvis på grunn av hydrogenbinding. Obligasjoner kan bli brutt i rett hår, og reformert (sammen med sulfid-bindinger) for å produsere krøllet hår.
