Hvordan beregne antall ledige stillinger i Copper

Elektroner få bygget opp i atomer i "skall". Hvert skall kan inneholde et visst antall elektroner. Hvis et skall ikke er full, er de tomme stedene kalles "ledige stillinger". Det er to enkle måter å beregne antall ledige stillinger i kobberatomene. Først starter fra den kjente elektroniske strukturen og telle antall tomrom i skallene. For det andre, se på plass i den periodiske tabellen og telle det antall plasser før skallene er fulle.
Bruksanvisning
Fra elektronisk konfigurasjon
1 Slå opp elektronisk konfigurasjon av kobber. Du finner det å være 1S2 / 2s2-2p6 / 3s2-3p6-3d10 / 4S1.
2 Recall eller slå opp antall elektroner som kreves for å fylle hver shell. Du vil finne s skjell for å være komplett 2 elektroner, p skjell på 6, og d skjell på 10.
3 Husker at stillinger er definert ved at de ytterste s og p skjell fylt, og telle antall gjenværende sporene i 4s og 4p skall av kobber. Siden 3d skallet er fylt, disse er de eneste gjenværende ledige stillinger. Så kobber har en elektron i 4s skallet, forlater en stilling, og ingen elektroner i 4p skallet, forlater 6 stillinger for totalt 7.
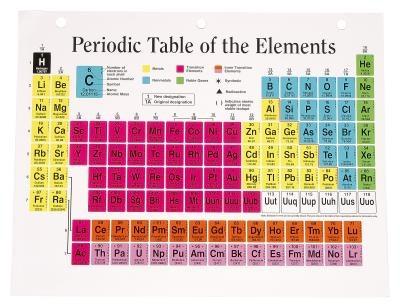
Fra posisjon på den periodiske tabell
Finne kobber i det periodiske system.
5 Huske at hver kolonne i det periodiske system representerer tilsetningen av en proton og en elektron til elementet i den foregående kolonne.
6 Husker at den kolonnen lengst til høyre representerer elementer med ingen ledige stillinger.
7 Tell antall kolonner fra kobber til slutten av sin rad på det periodiske system. Dette representerer antall elektroner som må legges for å nå en konfigurasjon med ingen ledige stillinger, så det er antall ledige stillinger i kobber. Finner man syv elementer fra kobber til krypton ved enden av raden.
Hint
- Elektroner liker å okkupere den lavest mulig energitilstand, men det er alle slags komplekse samspillet som gjør det vanskelig å foreta beregninger av den laveste energi neste tilgjengelige tilstand. De komplekse interaksjoner grunn for de to tilnærmingene er beskrevet her.