Hvordan forstå den periodiske Metals
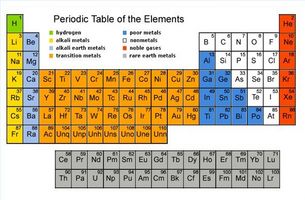
Den periodiske tabell er et vitenskapelig tabell som arrangerer de kjente metaller til en lettlest format. Den periodiske tabellen er hjørnesteinen til kjemi og vår forståelse av hvordan elementene reagerer med hverandre i naturen. Den første periodiske metaller er designet av Dmitrij Mendelejev i 1869 og inneholdt 65 av de kjente metaller. Den periodiske tabell over metaller inneholder nå 117 elementer eller metaller. Dmitrij Mendelejev arrangerte elementer ved atomvekt, med tyngre metall til venstre og elementer med liknende kjemiske egenskaper i samme kolonne. Den periodiske tabell over metaller kombinerer også metaller i lignende grupper. Disse gruppene er alkalimetaller, alkaliske jordmetaller, halogener, edelgasser, overgangsmetaller, sjeldne jordmetaller, andre metaller og andre ikke-jordmetaller.
Bruksanvisning
Begynn med å se på tabellen. Radene kalles perioder, og er oppført i rekkefølge av deres atomnummer fra lavest til høyest. Atomnummeret representerer antallet protoner som finnes i kjernen av deres atomer. Søylene er kalt grupper. Gruppene vurderes som de viktigste middel for å identifisere metaller. Grupperingene er kalt alkalimetaller, alkaliske jordmetaller, halogener, edelgasser, overgangsmetaller, sjeldne jordmetaller, andre metaller og andre ikke-jordmetaller. Gruppene indikerer lignende kjemiske egenskaper og den samme type av elektronkonfigurasjon i sin valens skall.
Elektronene i den ytre mantel er kalt valens elektroner, som bestemmer hvordan en reaktivt metall er til andre metaller. Romertallene ovenfor hver gruppe av elementer angir vanlige antall valenselektroner. Den "a" og "b" er inkludert ved siden av romertall bestemme hvor elektronene befinner seg. Representative elementene er "a" og deres elektroner bor i "s" og "p" undernivåer. Den ikke-representative elementene er "b" og sine elektroner bor i "d" og "F" undernivåer.
2 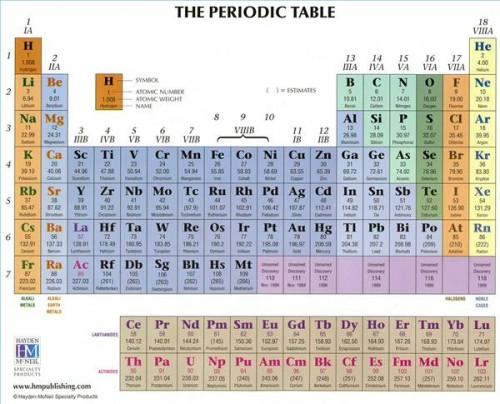
Se på tabellen og finn jern, eller Fe. Fe står for det latinske ordet Ferrum. Fe har en rekke tall rundt den. For å finne jern finne det i gruppe 8 VHIb. Ovenfor forkortelsen av Fe er dets atomnummer, som er 26. Vanligvis nedenfor Fe er atomvekten, som er 55,847. Noen periodesystemet varierer til en viss grad i informasjonen og konfigurasjon, men atomtall og atomvekt vil være tilstede.
3 Legg merke til en separat gruppe av metaller ved bunnen. Denne gruppen kalles sjeldne jordmetaller. De fleste av de sjeldne jordmetaller er menneskeskapt. Det er 30 av disse metallene, og de bor i gruppe 3 i rader 6 og 7. Disse metallene består av to serier av metaller kalt lantanid og actinide.