Definisjon av Infinite Fortynning
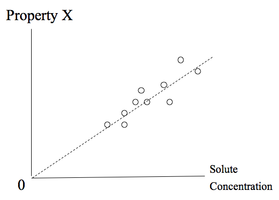
I kjemi, begrepet "uendelig fortynning" er et begrep som anvendes i studiet av løsemidler og oppløste stoffer (de stoffer som er oppløst i oppløsningsmidler). Det er en ekstrapoleringsmetoden, benyttes for å teste om en gitt egenskap ved en oppløsning stammer fra det oppløste stoff. Den esoteriske natur av test i kontrast med den beryktet den har mottatt i de siste tiår på grunn av sin sporadiske feil anvendelse innen medisin homøopatisk.
Strategi
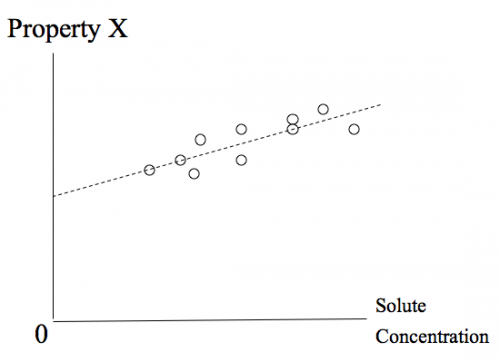
Uendelig fortynning er en test ved ekstrapolering, ikke en fysisk konsept. Det oppløste stoff er faktisk ikke reduseres til null konsentrasjon, for noen praktiske grunner. I stedet, en ekstrapolering, eller grense, blir bestemt fra datapunkter av forskjellige oppløste konsentrasjoner for å se om noe gitt egenskap ville forsvinne ved null oppløst stoff konsentrasjon. Hvis den gjør det, da eiendommen er forårsaket av oppløst stoff. Hvis ikke, blir det tatt som et bevis på at den observerte effekten skyldes noe annet enn den bestemte oppløste substans.
Noen definisjoner
Noen definisjoner for uendelig fortynning har blitt lagt frem i litteraturen. Man sier at uendelig fortynning er den spesielle oppførselen til en to-stoffblanding når konsentrasjonen av en komponent nærmer seg grensen for 0, og den andre nærmer seg en molfraksjon av en (den andre komponent er det løsningsmiddel).
En annen definisjon er: en bestemt atferd når blandingen er tilstrekkelig fortynne at oppløst stoff-oppløste interaksjoner er ubetydelig.
Rolle i å finne en Computational Base
I tillegg til å teste hvorvidt et oppløst materiale spiller en rolle i noen egenskap, kan uendelig fortynning metoden brukes for et par av andre grunner.
Som et eksempel er oppløseligheten gass avhengig av trykk og temperatur. Ved å bestemme løseligheten gass i grensen som det oppløste stoff konsentrasjonen går til null, kan en trykk- og temperatur-uavhengig basis lesning av oppløselighet gass bestemmes. Basen kan så bli modifisert for trykk- og temperatur-avhengighet ved høyere konsentrasjoner. Bruken av en base og separate modifiseringsfaktorer forenkler faktisk beregninger.
Forskning er også gjort i uendelig fortynning serien, det vil si, ved lave konsentrasjoner, ettersom området er vesentlig i flere industrier. For eksempel, i miljøindustrien, kan fjerne spormengder av forurensninger krever kjennskap til løsnings oppførsel ved lave konsentrasjoner. Rensing i den farmasøytiske industrien krever også kjennskap til virkemåten i dette område. Gummiindustrien er interessert i oppførselen til løsemidler når de kommer ut polymerer.
prosessuelle spørsmål
Men hvorfor bruke uendelig fortynning i det hele tatt? Hvorfor ikke bare teste et oppløsningsmiddel, uten at det oppløste stoffet oppløst i det?
I noen tilfeller er mer enn ett oppløst stoff til stede. Men så hvorfor ikke bare forberede et løsemiddel med bare de andre oppløste stoffer? Fordi de andre oppløste stoffer kan endre seg inn i nevnte oppløste stoff, for å oppnå dynamisk likevekt. Med andre ord, kan de være på motsatte sider av den samme kjemiske ligning. Svært få kjemiske reaksjoner skjer i bare en retning; de fleste reaksjoner er reversible. Så snart noen produktmolekyler danner begynner reverse reaksjonen skal finne sted. Eller de andre oppløste stoffer kan være nødvendig på en eller annen måte.
Poenget med forsøk kan ikke engang være å bestemme oppførselen ved fortynning grensen, men i stedet for å bestemme en beregnings base, som nevnt ovenfor.
Noen ganger er det ganske enkelt er ønskelig å være i stand til å identifisere og derfor eliminere bakgrunnsstøy fra oppløsningsmiddel-oppløsningsmiddel interaksjoner og andre kilde for å trekke ut fra etterfølgende beregninger av oppløst stoff oppførsel.
Totalt sett er den generelle ideen om at situasjonen er så komplekst at eliminering av en enkelt løst stoff er ikke en tilstrekkelig analyse. Et eksempel nedenfor illustrerer en slik komplikasjon.
Misbruk
Innenfor kjemisk forskning samfunnet, er subtile konsepter noen ganger ikke adressert tilstrekkelig, for eksempel using ekstrapolering å bestemme innholdet av lav konsentrasjon atferd eller forut ubetydelig ion samhandling på en utilstrekkelig lav konsentrasjon.
Uendelig fortynning overgrepene som får oppmerksomhet i media, men sentrum rundt homøopatisk samfunnet. I over et århundre, har medlemmer av homøopatisk samfunnet solgt fortynninger av giftstoffer, guidet av "lov om similars": hva gir symptomer i en frisk person vil kurere en syk person med symptomer. En rekke fortynninger ble funnet å redusere bivirkninger, uten å redusere virkningen av stoffet. (Tidligere og nåværende utøvere noen ganger fortynne giften så mye at det overstiger det som kalles fortynningen grensen, det punkt hvor det er lite sannsynlig at noen molekyler av det opprinnelige stoffet forblir --- bokstavelig talt et uendelig fortynning!)
Forskjellen fra den uendelige fortynning metode i kjemi --- bortsett fra å fysisk fortynne selv forbi fortynning grensen, i motsetning til ved hjelp av ekstrapolering --- er at disse utøverne mener at fordelen er konstant etter kraftig utvanning betyr vann / alkohol løsemiddel "lært "giften / aktiv ingrediens eiendommer. En kjemiker vil konkludere med det motsatte: at virkestoffet ikke har en fordel, og at et søk etter kilden til nytte ville bli funnet andre steder, for eksempel løsemidler, noen urenhet eller placebo effekt. Manglende evne til dem utenfor homeopati å gjenskape de gode resultatene av slike potions antyder en fjerde mulighet.
